酸化 力 の 強 さ - 酸化剤・還元剤の強さ|化学基礎【高校化学Net参考書】
ハロゲンの酸化力の強さを調べる実験
したがって、イオン半径の大きさが大きいほど、水酸化物イオン OH - とのクーロン力が弱くなり、水酸化物イオン OH - に負電荷が局在化することになるのです。
酸化剤とは? 酸化のはたらきをする物質とは?
・新・化学ノート 「3. 最後に・・・ 酸の強さと酸化力について、違いを教えてください。
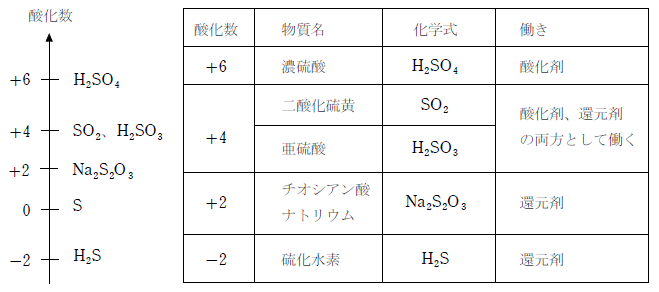
酸化剤・還元剤の強さ|化学基礎【高校化学Net参考書】
10 誘起効果 + I 効果 により非共有電子対が不安定化する このように誘起効果には、電子求引性の置換基と電子供与性の置換基の 2 種類があり、前者の誘起効果を特に - I 効果、後者の誘起効果を + I 効果といいます。
「酸化力が強い」って?
このOが共有電子ついを奪い取る という考え方は非常によく使います。
無機化学ハロゲン単体のまとめ!酸化力の強さが鍵
5 酸の相対的な強さ iii ルイスの定義 ルイスの定義における酸と塩基は、ブレンステッドの定義をさらに拡張して、電子対の供与と享受で定義しました。
強酸性と強酸化力はどう違う?酸化力を持つ酸の原因究明!
ですが、 普通の濃硫酸にはない、 加熱したときだけ持つ、 『 強酸化力』 これの真相は何なのでしょうか?濃硫酸が持つ酸化力では無いのか? 厳密に言うと、 濃硫酸に酸化力があるわけではないです。
ハロゲンの酸化力の強さを調べる実験
また、電気陰性度が大きいほど、一般的に電子親和力も大きくなる傾向があるので、酸 HA の共役塩基 A - が安定化します。
化学についてです。 酸化力が強いとは、自身が酸化が起こりやすいとい
アレニウスは、このような電解質の電離の理論に関する業績により、 1903 年にノーベル化学賞を受賞しています。
- 関連記事
2021 www.proinnovate.co.uk